内蒙古大学:《分析化学》课程教学资源(PPT课件)第八章 分析化学中的分离技术 第二节 沉淀分离法

第二章 一、无机沉淀剂沉淀分离 分析化学中的 法 分离技术 二、有机试剂沉淀分离法 三、盐析法 第二节 沉淀分离法 下页 帽財 越回 2024/19/13
2024/9/13 第二章 分析化学中的 分离技术 一、 无机沉淀剂沉淀分离 法 二、 有机试剂沉淀分离法 三、 盐析法 第二节 沉淀分离法
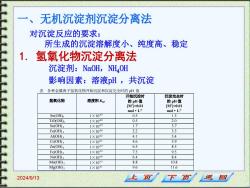
无机沉淀剂沉淀分离法 对沉淀反应的要求: 所生成的沉淀溶解度小、纯度高、稳定 1. 氢氧化物沉淀分离法 沉淀剂:NaOH,NH4OH 影响因素:溶液pH,共沉淀 表各种金属离子氢氧化物开始沉淀和沉淀完全时的pH值 开始沉淀时 沉淀完全时 氢氧化物 溶度积KsP 的pH值 的pH值 M=0.01 M1=0.01 mol·L1 mol·L Sn(OH)4 1×1037 0.5 1.3 TiO(OH)2 1×1029 0.5 2.0 Sn(OH)2 1×1027 1.7 3.7 Fe(OH)3 1×1038 2.2 3.5 Al(OH) 1×102 4.1 5.4 Cr(OH)3 1×1031 4.6 5.9 Zn(OH) 1×1017 6.5 8.5 Fe(OH), 1×109 7.5 9.5 Ni(OH)2 1×1018 6.4 8.4 Mn(OH)> 1×1013 8.8 10.8 Mg(OH)2 1×10n 9.6 11.6 2024/9/13 上页 下页 返回
2024/9/13 一、无机沉淀剂沉淀分离法 对沉淀反应的要求: 所生成的沉淀溶解度小、纯度高、稳定 1. 氢氧化物沉淀分离法 沉淀剂:NaOH,NH4OH 影响因素:溶液pH ,共沉淀 表 各种金属离子氢氧化物开始沉淀和沉淀完全时的 pH 值 氢氧化物 溶度积 KSP 开始沉淀时 的 pH 值 [M+ ]=0.01 mol·L -1 沉淀完全时 的 pH 值 [M+ ]=0.01 mol·L -1 Sn(OH)4 1×10-57 0.5 1.3 TiO(OH)2 1×10-29 0.5 2.0 Sn(OH) 2 1×10-27 1.7 3.7 Fe(OH) 3 1×10-38 2.2 3.5 Al(OH) 3 1×10-32 4.1 5.4 Cr(OH) 3 1×10-31 4.6 5.9 Zn(OH) 2 1×10-17 6.5 8.5 Fe(OH) 2 1×10-15 7.5 9.5 Ni(OH) 2 1×10-18 6.4 8.4 Mn(OH) 2 1×10-13 8.8 10.8 Mg(OH) 2 1×10-11 9.6 11.6
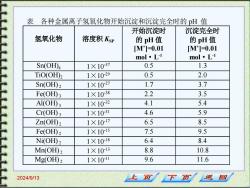
表各种金属离子氢氧化物开始沉淀和沉淀完全时的pH值 开始沉淀时 沉淀完全时 氢氧化物 溶度积KsP 的pH值 的pH值 [M]=0.01 [M]=0.01 mol·L4 mol·L1 Sn(OH)4 1×10-57 0.5 1.3 TiO(OH)2 1×10-29 0.5 2.0 Sn(OH)2 1×10-27 1.7 3.7 Fe(OH)3 1×10-38 2.2 3.5 Al(OH)3 1×10-32 4.1 5.4 Cr(OH)3 1×10-31 4.6 5.9 Zn(OH2 1×10-17 6.5 8.5 Fe(OH)2 1×10-15 7.5 9.5 Ni(OH)2 1×10-18 6.4 8.4 Mn(OHD)2 1×10-13 8.8 10.8 Mg(OH)2 1×10-川 9.6 11.6 2024/9/13 上页 下页 返回
2024/9/13 表 各种金属离子氢氧化物开始沉淀和沉淀完全时的 pH 值 氢氧化物 溶度积 KSP 开始沉淀时 的 pH 值 [M+ ]=0.01 mol·L -1 沉淀完全时 的 pH 值 [M+ ]=0.01 mol·L -1 Sn(OH)4 1×10-57 0.5 1.3 TiO(OH)2 1×10-2 9 0.5 2.0 Sn(OH) 2 1×10-27 1.7 3.7 Fe(OH) 3 1×10-3 8 2.2 3.5 Al(OH) 3 1×10-3 2 4.1 5.4 Cr(OH) 3 1×10-3 1 4.6 5.9 Zn(OH) 2 1×10-17 6.5 8.5 Fe(OH) 2 1×10-1 5 7.5 9.5 Ni(OH) 2 1×10-1 8 6.4 8.4 Mn(OH) 2 1×10-1 3 8.8 10.8 Mg(OH) 2 1×10-11 9.6 11.6

2.硫化物沉淀分离法 沉淀剂:H2S 约40余种金属离子可生成难溶硫化物沉淀; 各种金属硫化物沉淀的溶解度相差较大; 根据H,S的分布曲线,溶液中S2的浓度与pH有关,控制 溶液pH可控制分步沉淀。 H2S有毒,气味难闻; 选择性差。 2024/9/13 上页 下页返回
2024/9/13 2.硫化物沉淀分离法 沉淀剂:H2S 约40余种金属离子可生成难溶硫化物沉淀; 各种金属硫化物沉淀的溶解度相差较大; 根据H2S的分布曲线,溶液中S 2-的浓度与pH有关,控制 溶液pH 可控制分步沉淀。 H2S 有毒,气味难闻; 选择性差

有机试剂沉淀分离法 高选择性、高灵敏度;应用普遍; 有机沉淀剂与金属离子生成的三种沉淀类型: 1.螯合物沉淀 8-羟基喹啉与Mg2+生成六元环结构的螯合物沉淀; 在氨缓冲溶液中,可实现镁与碱金属及碱土金属的分离; 2.缔合物沉淀 四苯基硼化物与K的反应产物;溶度积2.25×10-8; 3.三元配合物沉淀 提高选择性和灵敏度的一条途径 2024/9/13 下页 返回
2024/9/13 二、有机试剂沉淀分离法 高选择性、高灵敏度;应用普遍; 有机沉淀剂与金属离子生成的三种沉淀类型: 1.螯合物沉淀 8-羟基喹啉与Mg2+生成六元环结构的螯合物沉淀; 在氨缓冲溶液中,可实现镁与碱金属及碱土金属的分离; 2.缔合物沉淀 四苯基硼化物与K +的反应产物;溶度积2.25×10-8; 3.三元配合物沉淀 提高选择性和灵敏度的一条途径;

三、盐析法 在溶液中加入中性盐使溶质生成沉淀析出; 易产生共沉淀,选择性差; 成本低,简便; 蛋白质的分离:对其生物活性有稳定作用; 常用的中性盐:疏酸盐、磷酸盐、氯化物等;在蛋白质 的分离中硫酸铵、硫酸钠应用较多。 2024/9/13 上页 下页 返回
2024/9/13 三、盐析法 在溶液中加入中性盐使溶质生成沉淀析出; 易产生共沉淀,选择性差; 成本低,简便; 蛋白质的分离:对其生物活性有稳定作用; 常用的中性盐:硫酸盐、磷酸盐、氯化物等;在蛋白质 的分离中硫酸铵、硫酸钠应用较多

内容选择 第一节概述 第二节沉淀分离法 第三节溶剂萃取分离法 第四节离子交换分离法 第五节膜分离技术与生物试样分离 结束 2024/9/13 上页 下不页 返回
2024/9/13 内容选择 第二节 沉淀分离法 第三节 溶剂萃取分离法 第四节 离子交换分离法 第五节 膜分离技术与生物试样分离 结束 第一节 概述
按次数下载不扣除下载券;
注册用户24小时内重复下载只扣除一次;
顺序:VIP每日次数-->可用次数-->下载券;
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第八章 分析化学中的分离技术 第一节 概述.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第七章 色谱分析法 第九节 高效毛细管电泳.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第七章 色谱分析法 第八节 离子色谱法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第七章 色谱分析法 第七节 液相色谱法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第七章 色谱分析法 第六节 毛细管色谱法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第七章 色谱分析法 第三节 色谱理论基础.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第一章 绪论 第二节 分析化学的分类与进展.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第七章 色谱分析法 第二节 气相色谱仪.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第七章 色谱分析法 第一节 色谱法概述.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第六章 原子吸收分析法 第四节 条件选择与定量方法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第六章 原子吸收分析法 第三节 干扰及其消除.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第六章 原子吸收分析法 第二节 原子吸收分光光度仪.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第六章 原子吸收分析法 第一节 原子吸收分析原理.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第五章 分光光度分析法 第五节 有机物紫外光谱解析.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第五章 分光光度分析法 第四节 分光光度测量方法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第五章 分光光度分析法 第三节 显色与测量条件的选择.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第一章 绪论 第一节 分析化学的作用.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第五章 分光光度分析法 第一节 光度法基本原理.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第四章 电化学分析法 第六节 电导分析法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第四章 电化学分析法 第五节 极谱与伏安分析法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第一章 绪论 第三节 其他.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第八章 分析化学中的分离技术 第三节 溶剂萃取分离法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第八章 分析化学中的分离技术 第四节 离子交换分离法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第八章 分析化学中的分离技术 第五节 膜分离技术.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第九章 红外光谱分析 第一节 红外基本原理.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第九章 红外光谱分析 第二节 红外光谱仪器.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第九章 红外光谱分析 第四节 红外谱图解析示例.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第十章 核磁共振波谱分析 第一节 核磁共振基本原理.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第十章 核磁共振波谱分析 第二节 核磁共振与化学位移.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第十章 核磁共振波谱分析 第三节 自旋偶合与自旋裂分.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第二章 定量分析中的误差与数据处理 第一节 定量分析中的误差.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第十章 核磁共振波谱分析 第四节 谱图解析与结构确定.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第十一章 质谱分析 第一节 基本原理与质谱仪.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第十一章 质谱分析 第二节 离子峰的主要类型.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第十一章 质谱分析 第三节 有机分子裂解类型.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第十一章 质谱分析 第四节 质谱图与结构解析.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第二章 定量分析中的误差与数据处理 第二节 分析结果的数据处理.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第二章 定量分析中的误差与数据处理 第三节 数据评价方法.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第二章 定量分析中的误差与数据处理 第四节 有效数字与运算规则.ppt
- 内蒙古大学:《分析化学》课程教学资源(PPT课件)第二章 定量分析中的误差与数据处理 第五节 线形方程拟合.ppt
