上饶师范学院:《无机化学》课程电子教案(课件讲稿)第十四章 氮族元素

氮族元素 氮族通性 氮及其化合物 磷及其化合物 砷锅 盐类的热分解 本章要求
氮族元素 氮 族 通 性 氮 及 其 化 合 物 磷 及 其 化 合 物 砷 锑 铋 盐 类 的 热 分 解 作 业 本 章 要 求

氮族通性 化基本上 髯铋的一 勺对象。 )、磷 )和铋 舍勒(用 舍勤,CW. 验的仪器
在非金属化学中,氮族元性质的变化基本上 是规律的,是由典型非金属氮到典型金属铋的一 个完整过渡,因此往往被选为系统研究的对象。 周期系第VA族元素,包括了氮(Nitrogen)、磷 (Phosphorus)、砷(Arsenic)、锑(Stibium)和铋 (Bismuth)。 一、元素的发现 氮由英-卢塞福、普利斯特里、瑞典-舍勒(用 NaOH除空气中的CO2,P除O2)所发现。 氮族通性

氮族通性 第一个发现磷的是德国的波兰特,他听到一“尿 里可制得黄金”这样一句传说。他就抱着发财的目地, 用尿做了大量实验,1669年他在一次实验中用砂、木 炭、石灰等和尿混合,加热蒸馏,虽没得到黄金却意 外地得到一种美丽的物质,它色白质软,在黑暗的地 方能发光,取名“冷光”,起初他极守密,不过此消 息立刻传遍了德国。 砷是由中国的炼丹家葛洪发现的(317年),德 国的A.Magnus在(1250年)也得到了砷。 锑是古代发现的。 铋是由法国的C.J.Geoffroy.从铅中分离得到的
氮族通性 第一个发现磷的是德国的波兰特,他听到-“尿 里可制得黄金”这样一句传说。他就抱着发财的目地, 用尿做了大量实验,1669年他在一次实验中用砂、木 炭、石灰等和尿混合,加热蒸馏,虽没得到黄金却意 外地得到一种美丽的物质,它色白质软,在黑暗的地 方能发光,取名“冷光”,起初他极守密,不过此消 息立刻传遍了德国。 砷是由中国的炼丹家葛洪发现的(317年),德 国的A.Magnus在(1250年)也得到了砷。 锑是古代发现的。 铋是由法国的C.J.Geoffroy从铅中分离得到的

氮族通性 二、氮族元素的基本性质 性质 N P As Sb Bi 原子序数 7 15 33 51 83 原子量 14.01 30.97 74.92 121.75 208.98 共价半径pm 55 110 121 141 154.7 离子 T 171 212 222 245 - 半径 T 16 44 58 76 98 /pm MS 13 35 46 62 74 第一电离势 1402 1011.8 859.7 833.7 703.3 (KJ/mol) 第一电子亲和 -7 71.7 77 101 100 势(KJ/mol) 电负性 3.04 2.19 2.18 2.05 2.02
氮族通性 性 质 N P As Sb B i 原子序数 7 15 33 51 83 原子量 14.01 30.97 74.92 121.75 208.98 共价半径/pm 55 110 121 141 154.7 M 3- 171 212 222 245 - M 3+ 16 44 58 76 98 离 子 半 径 /pm M 5+ 13 35 46 62 74 第一电离势 (KJ/mol) 1402 1011.8 859.7 833.7 703.3 第一电子亲和 势(KJ/mol) -7 71.7 77 101 100 电负性 3.04 2.19 2.18 2.05 2.02 二、氮族元素的基本性质
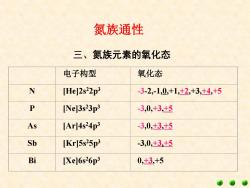
氮族通性 三、氮族元素的氧化态 电子构型 氧化态 N [He]2s22p3 -3-2,-1,0,+1,+2,+3,+4,+5 P [Ne]3s23p3 -3,0,+3,+5 As [Ar]4s24p3 -3,0,+3,+5 Sb [Kr]5s25p3 -3,0,+3.+5 Bi [Xe]6s26p3 0,+3,+5
氮族通性 电子构型 氧化态 N [He]2s 22p 3 -3-2,-1,0,+1,+2,+3,+4,+5 P [Ne]3s 23p 3 -3,0,+3,+5 As [Ar]4s 24p 3 -3,0,+3,+5 Sb [Kr]5s 25p 3 -3,0,+3,+5 Bi [Xe]6s 26p 3 0,+3,+5 三、氮族元素的氧化态

氮族通性 四、氮族元素的特性 由于价电子层为ns2np3与氧族、卤素比较,它们 若要获得三个电子而形成-Ⅲ价的离子是较困难的, 只有电负性较大的N、P能形成极少数-Ⅲ价的离子型 化合物,LiN、Mg3N2、Na3P、Ca3P,等,由于N3-、 P3离子半径大容易变型,遇水强烈水解生成NH和 PH3如: Mg3N2+6H2O===3Mg(OH)2+3NH3T Na3P+3H2O===3NaOH+3PH3T 本族元素形成正价的趋势较强,如NF3、PBrs AsFs、SbCIs、BiCL3、SbCl等,形成共价化合物是 本族元素的特征
氮族通性 四、氮族元素的特性 由于价电子层为ns2np3与氧族、卤素比较,它们 若要获得三个电子而形成-Ⅲ价的离子是较困难的, 只有电负性较大的N、P能形成极少数-Ⅲ价的离子型 化合物,Li3N、Mg3N2、Na3P、Ca3P2等,由于N3-、 P3-离子半径大容易变型,遇水强烈水解生成NH3和 PH3如: Mg3N2+6H2O===3Mg(OH)2+3NH3 Na3P+3H2O===3NaOH+3PH3 本族元素形成正价的趋势较强,如NF3、PBr5、 AsF5、SbCl5、BiCl3、SbCl3等,形成共价化合物是 本族元素的特征

氮族通性 从N到Bi,+V氧化态的稳定性递减,而+Ⅲ氧化态 的稳定性递增。 +V氧化态的氮是较强的氧化剂。除氮外从磷到 铋+V氧化态的氧化性(从+V还原到+Ⅲ)依次增强。 +V氧化态的磷儿乎不具有氧化性并且最稳定,而 +V氧化态的铋是最强的氧化剂,它的+Ⅲ氧化态最稳 定,几乎不显还原性
氮族通性 从N到Bi,+V氧化态的稳定性递减,而+Ⅲ氧化态 的稳定性递增。 +V氧化态的氮是较强的氧化剂。除氮外从磷到 铋+V氧化态的氧化性(从+V还原到+Ⅲ)依次增强。 +V氧化态的磷儿乎不具有氧化性并且最稳定,而 +V氧化态的铋是最强的氧化剂,它的+Ⅲ氧化态最稳 定,几乎不显还原性

氨及其化合物 氮 氨 氨的衍生物 氮的氧化物 亚硝酸及其盐 硝酸及其盐 光化学烟雾
氮及其化合物 氮 光 化 学 烟 雾 氨 氨 的 衍 生 物 氮 的 氧 化 物 亚硝酸及其盐 硝 酸 及 其 盐

氮 工业上生产氮一般是由分馏液态空气在15.2MPa (150atm)压力下装入钢瓶备用。或做成液氮存于液氮 瓶中,实验室里备少量氮气。如: NuNn饱和)==NHNO2+NaCl 液态氨的 ,N2↑+2H20 沸点为77K,能 产生很低的温 NO、O2和H,0等杂质,可设 度,是最常用 △-N2↑+Cr203+4H20 的致冷剂。 =3Cu+N2↑+3H20 NaN3=Na①⑩+N2↑(可得到很纯的氮)
氮 工业上生产氮一般是由分馏液态空气在15.2MPa (150atm)压力下装入钢瓶备用。或做成液氮存于液氮 瓶中,实验室里备少量氮气。如: NaN3===Na(l)+N2(可得到很纯的氮) 产物中有少量NH3、NO、O2和H2O等杂质,可设 法除去。 (NH4 )2Cr2O7===N2+Cr2O3+4H2O 2NH3+3CuO===3Cu+N2+3H2O NH4Cl(s)+NaNO2 (饱和)===NH4NO2+NaCl NH4NO2===N2+2H2O

氮 氮原子间能形成多重键,因而能生成本族其它元 素所没有的化合物如叠氮化物N3),偶氮化合物(一N =N一)等。由于N2的键能很大(946kJmo),加热到 3273K时,只有0.1%离解。 N2在常温下就和锂直接反应生成Li,N,在高温时 不但能和镁、钙、铝、硼、硅等化合生成氮化物,而 且能与氧、氢直接化合。 因的原子半径小、又没有d轨道可供成键,所以 N在化合物中的配位数最多不超过4
氮 氮原子间能形成多重键,因而能生成本族其它元 素所没有的化合物如叠氮化物(N3 - ),偶氮化合物(—N =N—)等。由于N2的键能很大(946kJ·mol-1 ),加热到 3273K时,只有0.1%离解。 N2在常温下就和锂直接反应生成Li3N,在高温时 不但能和镁、钙、铝、硼、硅等化合生成氮化物,而 且能与氧、氢直接化合。 因N的原子半径小、又没有d轨道可供成键,所以 N在化合物中的配位数最多不超过4
按次数下载不扣除下载券;
注册用户24小时内重复下载只扣除一次;
顺序:VIP每日次数-->可用次数-->下载券;
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第十五章 碳族元素(碳、硅、硼).pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第十二章 卤素.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第十三章 氧族元素.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第十一章 氧化还原反应.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第十章 电解质溶液.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第八章 化学平衡.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第九章 溶液.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第六章 化学热力学初步.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第五章 氢、稀有气体.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第七章 化学反应速度.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第四章 化学键与分子结构.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第三章 原子结构.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第二章 物质的状态.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第一章 绪论.pdf
- 上饶师范学院:《无机化学》课程教学资源(习题解答)期末考试模拟试卷(上册,共十套,含答案).pdf
- 上饶师范学院:《无机化学》课程教学资源(习题解答)第20章 d区金属(二)第五、六周期d区金属.pdf
- 上饶师范学院:《无机化学》课程教学资源(习题解答)第17章 P区金属.pdf
- 安徽科技学院:《分析化学》课程电子教案(PPT课件,基础分析)第八章 吸光光度法.ppt
- 安徽科技学院:《分析化学》课程电子教案(PPT课件,基础分析)第七章 沉淀滴定法.ppt
- 安徽科技学院:《分析化学》课程电子教案(PPT课件,基础分析)第六章 氧化还原滴定法.ppt
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第十七章 碱金属与碱土金属.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第十八章 铜、锌副族.pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第二十章 过渡元素(一).pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第二十一章 过渡元素(二).pdf
- 上饶师范学院:《无机化学》课程电子教案(课件讲稿)第二十二章 镧系元素和锕系元素.pdf
- 和频光谱在生物膜等生物界面中的应用 In situ molecular level studies on membrane related peptides and proteins in real time using sum frequency generation vibrational spectroscopy.pdf
- 中国科学技术大学:《高分子化学》课程教学资源(课件讲稿)第六、七、八、九章 离子聚合、开环聚合、链式共聚合反应、配位聚合、聚合物的化学反应(主讲:刘世勇).pdf
- 厦门大学:《量子化学 Quantum Chemistry》课程电子教案(教学课件)Chapter 1 Schrödinger 方程 Schrodinger equation.ppt
- 厦门大学:《量子化学 Quantum Chemistry》课程电子教案(教学课件)Chapter 2 简单量子力学体系 Rudimental quantum mechanics system.ppt
- 厦门大学:《量子化学 Quantum Chemistry》课程电子教案(教学课件)Chapter 3 矩阵与算符 Matrix and operator.ppt
- 厦门大学:《量子化学 Quantum Chemistry》课程电子教案(教学课件)Chapter 4 角动量与自旋 Angle momentum and spin.ppt
- 厦门大学:《量子化学 Quantum Chemistry》课程电子教案(教学课件)Chapter 5 原子结构 Atomic structure.pdf
- 厦门大学:《量子化学 Quantum Chemistry》课程电子教案(教学课件)Chapter 6 分子的对称性与对称群 Molecular symmetry and symmetric group.pdf
- 厦门大学:《量子化学 Quantum Chemistry》课程电子教案(教学课件)Chapter 7 简单分子轨道理论 Elementary molecular orbital(MO)theory.pdf
- 厦门大学:《量子化学 Quantum Chemistry》课程电子教案(教学课件)Chapter 8 共轭分子的结构与性能 Ab initio technique for polyatomic molecular.pdf
- 厦门大学:《量子化学 Quantum Chemistry》课程电子教案(教学课件)Chapter 9 多原子的半经验方法 Semi-experimental method for polyatomic molecular.ppt
- 厦门大学:《结构化学 Structural Chemistry》课程教学资源(课件讲稿)Chapter 1 The Basic Knowledge of Quantum Mechanics(讲授:曹泽星、蒋亚琪).pdf
- 厦门大学:《结构化学 Structural Chemistry》课程教学资源(课件讲稿)Chapter 2 Atomic Structure.pdf
- 厦门大学:《结构化学 Structural Chemistry》课程教学资源(课件讲稿)Chapter 3 Molecular symmetry and symmetry point group.pdf
- 厦门大学:《结构化学 Structural Chemistry》课程教学资源(课件讲稿)Chapter 4 The structure of diatomic molecules.pdf
